熱線:021-56056830,66110819
手機:13564362870


熱線:021-56056830,66110819
手機:13564362870
2結果
2.1 N2O排放速率與累積排放量
本研究結果表明,土壤N2O排放速率隨著土壤含水量升高而增加(圖1-A)。在80%、95%WFPS條件下,各處理間土壤N2O排放速率在培養第2—4天出現排放高峰,并且其最大排放速率分別為1.46和3.30 mgN·kg-1·d-1,隨后N2O排放速率逐漸降低。67%WFPS土壤N2O整體排放水平比較低(低于0.20 mgN·kg-1·d-1),在培養第1—2天出現較高的N2O排放量。高、中和低含水量土壤N2O加權平均排放通量分別為1.17、0.27和0.08 mgN·kg-1·d-1。其中,高、中含水量土壤在培養前7—10 d具有較高的N2O排放速率,之后排放速率較低且變化不大。低含水量各處理間N2O排放速率差異顯著,且無C2H2處理>10%(V/V)C2H2處理>0.1%(V/V)C2H2處理(表1)。
整個培養周期,高、中和低含水量土壤N2O累積排放量分別為21.06、4.77和1.48 mgN·kg-1,分別為培養初期總的無機氮含量的19.39%、4.39%和1.36%(NH+4-N+NO-3-N初始含量均為108.62 mgN·kg-1),這說明,隨著土壤含水量增大,氣態氮損失量增加;高、中含水量土壤N2O累積排放量分別比低含水量高13.23和2.22倍,高含水量土壤N2O累積排放量比中含水量高3.42倍。各水分處理間N2O累積排放量均達到顯著水平(<0.01)。
各含水量土壤,無C2H2處理N2O累積排放量均顯著高于0.1%(V/V)C2H2處理(<0.01),這說明0.1%(V/V)C2H2處理有效抑制了硝化過程中的自養氨氧化過程;同時,10%(V/V)C2H2處理N2O累積排放量均顯著高于0.1%(V/V)C2H2處理(<0.01),這表明10%(V/V)C2H2處理有效抑制了N2O還原成N2的過程(表1)。
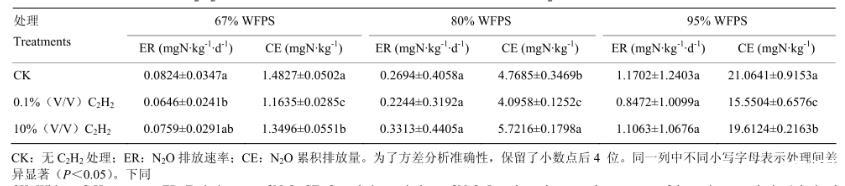
表1兩種C2H2處理對土壤N2O排放速率及累積排放量的影響
CK:無C2H2處理;ER:N2O排放速率;CE:N2O累積排放量。為了方差分析準確性,保留了小數點后4位。同一列中不同小寫字母表示處理間差異顯著(<0.05)。下同
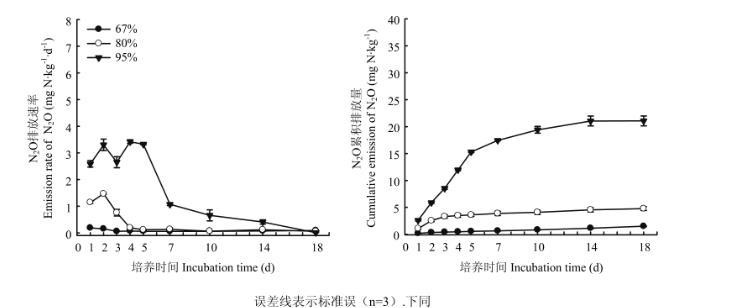
誤差線表示標準誤(n=3).下同
圖1不同含水量土壤培養期N2O排放速率和累積排放量
2.2土壤中無機氮NH+4-N和NO-3-N含量的變化
培養期間,土壤中NH+4-N和NO-3-N濃度變化說明了氮的轉化過程。各處理土壤NH+4-N濃度大體上均呈逐漸下降趨勢。中、低含水量處理,土壤NH+4-N濃度在培養開始后急劇下降,至培養第3天分別降低了95.54%和97.22%,之后稍有波動,但變化不大。高含水量處理NH+4-N濃度與另外兩個處理相比下降緩慢,到培養第3和10天分別減少了49.85%和77.89%(圖2-A)。
土壤NO-3-N含量在整個培養周期呈增加的趨勢。中、低含水量處理,土壤中NO-3-N濃度從培養開始至第3天迅速升高,之后未出現明顯變化。至培養第18天,高、中和低含水量處理NO-3-N濃度分別為80.66、101.54和100.03 mgN·kg-1(3個含水量NO-3-N初始含量均為6.29 mgN·kg-1),高含水量處理與中、低含水量處理間差異顯著(=0.0086),中低含水量處理間差異不顯著(圖2-B)。
2.3不同乙炔處理下反硝化產物N2O和N2O+N2的產生規律
N2O還原成N2的途徑對于了解農業土壤中N2O消耗非常重要,并且這可能是一個考慮如何減緩N2O排放的方向。0.1%(V/V)C2H2抑制自養氨氧化作用,10%(V/V)C2H2抑制N2O還原成N2,同時抑制自養氨氧化作用。本研究通過分析0.1%(V/V)C2H2和10%(V/V)C2H2處理組N2O排放通量來估測可能的反硝化產物(N2O+N2)排放量以及N2O/(N2O+N2)比率。培養期間,土壤反硝化作用產生的N2O和(N2O+N2)加權平均排放通量,高含水量處理(分別為0.85和1.11 mgN·kg-1·d-1)顯著高于中(分別為0.22和0.33 mgN·kg-1·d-1)、低含水量處理(分別為0.06和0.08 mg·N·kg-1·d-1),兩個較低含水量處理間也均達顯著水平(均為<0.0001;表1)。高、中和低含水量土壤N2O/(N2O+N2)比率分別為0.61、0.72和0.86,并且各水分處理間差異顯著(<0.0001),這說明,在67%WFPS處理下,只有14%的N2O還原成了N2,大部分以N2O形式排放到了外界環境中(表1)。
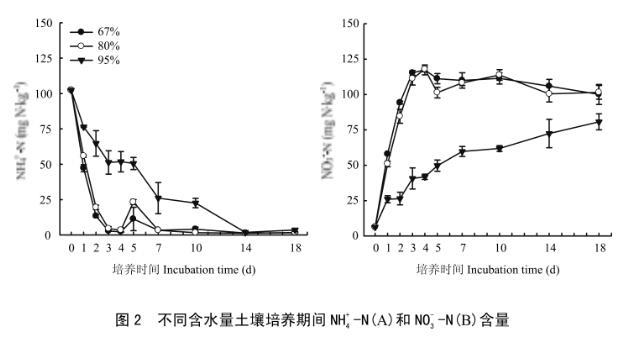
圖2不同含水量土壤培養期間NH+4-N(A)和NO-3-N(B)含量
2.4土壤N2O的同位素特征
N2O峰值一般出現在施肥后一周內。因此,以下探討了培養第一周期間N2O同位素特征。N2O同位素特征值受土壤含水量的影響顯著(圖3)。對于N2O的δ15Nbulk和δ18O,各含水量處理間差異均達顯著性水平(<0.0001)。高、低含水量處理的SP值顯著高于中含水量(<0.0001)。所有處理下δ15Nbulk平均值均為負值,變化范圍為從-43.95‰到-5.31‰,δ18O和SP平均值均為正值,變化范圍分別為12.28‰—40.66‰以及10.30‰—21.58‰。土壤含水量對N2O同位素特征值影響利用相關性進行分析發現,WFPS與δ15Nbulk具有顯著負相關關系(=-0.77,<0.0001),另外,其與δ18O和SP均無顯著相關性;SP與δ15Nbulk呈顯著正相關(=0.34,<0.01),與δ15Nbulk相比,SP與δ18O相關性更加顯著(=0.56,<0.0001);δ15Nbulk和δ18O具有顯著正相關關系(=0.61,<0.0001)。
土壤排放N2O的δ15Nbulk值隨著土壤含水量的增加而減小(圖3)。根據同位素分餾效應,添加NH+4會誘導土壤發生硝化作用,隨著硝化作用進行,剩余底物會富集重同位素,導致NH+4的δ15N增加,這可能會促使N2O的δ15Nbulk發生顯著變化,因此,可能會使利用δ15Nbulk區分N2O產生途徑復雜化。研究發現,3個含水量在無C2H2處理下N2O的δ15Nbulk在培養第一周均呈增加趨勢,變化范圍為-54.78‰—3.62‰,這與之前的研究一致,即施用尿素和銨態氮肥料后,N2O的δ15Nbulk通常會隨著培養時間升高。δ15Nbulk加權平均值為高含水量(-42.93‰)<中含水量(-28.81‰)<低含水量(-4.07‰),且各水分處理間差異顯著(<0.0001)。
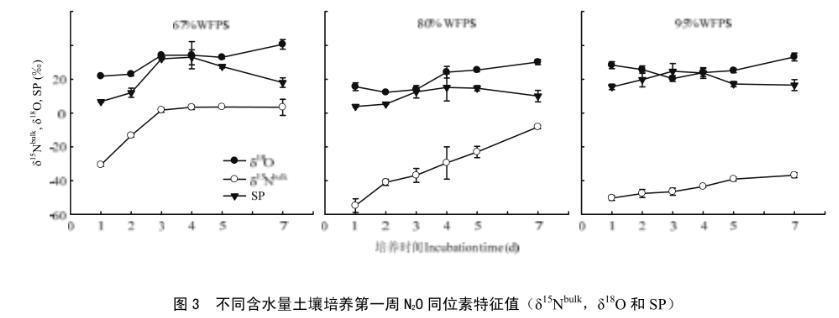
圖3不同含水量土壤培養第一周N2O同位素特征值(δ15Nbulk,δ18O和SP)
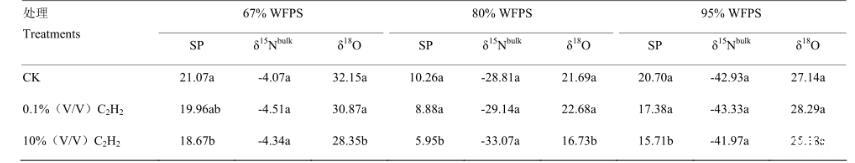
表2兩種C2H2處理對土壤N2O同位素特征值(δ15Nbulk,δ18O,SP)的影響
2.5基于SP值的硝化和反硝化過程對土壤N2O排放的貢獻率
不加C2H2各處理SP值在培養第一周均呈先升高再下降的趨勢(圖3)。高、中和低含水量土壤N2O的SP加權平均值,不加C2H2處理下分別為20.70‰、10.26‰和21.07‰,這與之前純培養研究相比,高于反硝化作用SP值(-10‰—0‰),低于硝化作用SP值(33‰—37‰),這說明在各含水量土壤中可能同時具有多個N2O產生途徑。0.1%(V/V)C2H2處理下高、中和低含水量的SP加權平均值分別為17.38‰、8.88‰和19.96‰,10%(V/V)C2H2處理下,高(15.71‰)、中(5.95‰)和低(18.67‰)含水量土壤N2O的SP加權平均值分別比0.1%(V/V)C2H2處理降低了10%、33%和6%。該結果表明,反硝化過程中可能發生N2O還原(表2)。低含水量處理的SP值在培養前兩天均較低(分別為6.74‰和12.04‰),以反硝化作用為主,分別占N2O生成量的66.15%和56.36%;之后主要以硝化作用為主;中含水量土壤的SP值在培養第1—7天均較低(3.92‰—15.21‰),N2O主要由反硝化作用產生,由反硝化作用排放的N2O貢獻率為40.90%—74.04%(表3);高含水量處理10%(V/V)C2H2的SP值在培養第一周比較高(7.61‰—21.11‰),而添加10%(V/V)C2H2處理會抑制自養氨氧化過程以及N2O還原成N2過程,故該處理不會因此出現較高的SP值,這說明可能發生了部分真菌反硝化作用。MAEDA等通過研究67種真菌發現其SP平均值為30‰±4.8‰(測得的SP值范圍為15.8‰—36.7‰)。
 相關新聞
相關新聞